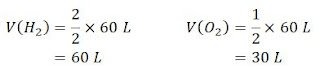Contoh Soal dan Pembahasan Lengkap Stoikoimetri Kimia (1) - Pada kesempatan kali ini kita akan mencoba membahas Contoh Soal dan Pembahasan Lengkap Stoikoimetri Kimia yang ada di kelas 10 SMA. Pada artikel sebelumnya kita sudah pernah membahas secara lengkap materi stoikiometri mulai dari mencari nilai mol, massa, volume dan lain-lain baik dalam senyawa atau masuk dalam persamaan reaksi. Pada pembahasan kita kali ini mungkin akan kita bagi menjadi beberapa bagian dikarenakan soal yang dibahas lumayan banyak.
 |
| Google Image - Contoh Soal dan Pembahasan Lengkap Stoikoimetri Kimia (1) |
Soal dan Pembahasan Stoikoimetri
Soal nanti dibawah kita ambil dari soal uji kemampuan tiap sub bab, dan di artikel selanjutnya kita akan mencoba ke evaluasi materi bab. Bagi teman Sains Seru yang mau memberikan soal tentang stoikiometri sendiri untuk di bahas disini bisa kirimkan ke kita langsung melalui contact atau bisa dengan tinggalkan di kolom komentar dibawah. Baik langsung saja kita mulai ya pembahasan soal stoikiometri.
Soal No 1.
Logam Aluminium sebanyak 27 g dibakar di udara. Tentukan massa gas oksigen yang diperlukan jika hasil reaksi berupa senyawa aluminium oksida (Al₂O₃).
Jawab
Sebelumnya kita tuliskan terlebih dahulu persamaan reaksinya.
4Al + 3O₂ → 2Al₂O₃ [setara]
Kita ketahui (Ar Al = 27, Ar O = 16)
Mr Al₂O₃ = (2 × Ar Al) + (3 × Ar O)
= (2 × 27) + (3 × 16)
= 54 + 48
= 102
Kita bisa menggunakan perbandingan, maka


Soal No 2.
Perhatikan persamaan reaksi berikut.
2H₂(g) + O₂(g) → 2H₂O(g) [setara]
Hitunglah volume gas hidrogen dan gas oksigen yang diperlukan untuk membuat 60 L air.
Jawab
Kita bisa mengunakan rumus perbandingan untuk menyelesaikan soal diatas.
Soal No 3.
Perhatikan persamaan reaksi berikut.
CH₄(g) + 2O₂(g) → CO₂(g) + 2H₂O(g) [setara]
Hitunglah volume gas oksigen yang dibutuhkan untuk membakar gas metana jika volume gas metana 10 L dan berapa volume gas CO₂ dan gas H₂O yang terbentuk?
Jawab
Caranya sama dengan soal no 2, yaitu dengan perbandingan seperti dibawah.
Baca juga Rumus perbandingan volume.
Soal No 4.
Sebanyak 4 L gas C₃H₈ dibakar habis dengan gas oksigen sesuai dengan persamaan reaksi.
C₃H₈(g) + 5O₂(g) → 3CO₂(g) + 4H₂O(g) [setara]
Hitunglah volume gas oksigen yang diperlukan serta volume gas karbon dioksida dan uap air jika pembakaran dilakukan pada suhu dan tekanan yang sama.
Jawab
Caranya masih sama, menggunakan perbandingan volume seperti dibawah ini.
Jadi, volume gas oksigen, volume gas karbon dioksida, dan uap air berturut-turut adalah 20 L, 12 L, dan 16 L.
Soal No 5.
Jika terdapat 6 L C₂H₆ (9 × 10²³ molekul) dibakar dengan gas oksigen menghasilkan gas karbon dioksida dan uap air, tentukanlah:
a. persamaan reaksi;
b. jumlah molekul gas oksigen;
c. jumlah molekul gas karbon dioksida;
d. jumlah molekul uap air;
e. volume gas oksigen;
f. volume gas karbon dioksida;
g. volume gas uap air.
JP (C₂H₆) = 9 × 10²³ molekul
a. Kita buat persamaan kimia yang setara ya, harapannya teman Sains Seru bisa membuatnya karena reaksi pembakaran pasti akan seperti dibawah ini yang membedakan hanya koefisien saja.
2C₂H₆(g) + 7O₂(g) → 4CO₂(g) + 6H₂O(g) [setara]
Untuk jawaban b sampai d bisa menggunakan rumus perbandingan jumlah partikel.
b. Rumus perbandingan jumlah molekul seperti dibawah ini.
Jadi, jumlah molekul gas oksigen sebesar 3,15 × 10²⁴ molekul.
c. Rumus perbandingan jumlah molekul seperti dibawah ini.
Jadi, jumlah molekul gas karbon dioksida sebesar 1,8 × 10²⁴ molekul.
d. Rumus perbandingan jumlah molekul seperti dibawah ini.
Jadi, jumlah molekul uap air sebesar 2,7 × 10²⁴ molekul.
Untuk jawaban e sampai g bisa menggunakan rumus perbandingan volume.
e. Rumus perbandingan volume seperti dibawah ini.
Jadi, volume gas oksigen sebesar 21 L.
f. Rumus perbandingan volume seperti dibawah ini.
Jadi, volume gas karbon dioksida sebesar 12 L.
g. Rumus perbandingan volume seperti dibawah ini.
Jadi, volume uap air sebesar 18 L.
Contoh soal No 6 sampai 10 dilanjut disini.
Contoh Soal dan Pembahasan Lengkap Stoikoimetri Kimia (1) - Mungkin sekian dulu ya Contoh Soal dan Pembahasan Stoikoimetri Kimia no 1 sampai 5. Semoga contoh soal dan pembahasan singkat diatas dapat bermanfaat bagi teman setia Sains Seru. Jika ada yang mau ditanyakan bisa tinggalkan di kolom komentar dibawah ya. Kita akan melanjutkan ke Evaluasi Materi BAB jadi ikuti terus ya update artikel disini ya. Terimakasih atas perhatiannya, See You.
a. persamaan reaksi;
b. jumlah molekul gas oksigen;
c. jumlah molekul gas karbon dioksida;
d. jumlah molekul uap air;
e. volume gas oksigen;
f. volume gas karbon dioksida;
g. volume gas uap air.
Jawab
Diket: V (C₂H₆) = 6 LJP (C₂H₆) = 9 × 10²³ molekul
a. Kita buat persamaan kimia yang setara ya, harapannya teman Sains Seru bisa membuatnya karena reaksi pembakaran pasti akan seperti dibawah ini yang membedakan hanya koefisien saja.
2C₂H₆(g) + 7O₂(g) → 4CO₂(g) + 6H₂O(g) [setara]
Untuk jawaban b sampai d bisa menggunakan rumus perbandingan jumlah partikel.
b. Rumus perbandingan jumlah molekul seperti dibawah ini.
Jadi, jumlah molekul gas oksigen sebesar 3,15 × 10²⁴ molekul.
c. Rumus perbandingan jumlah molekul seperti dibawah ini.
Jadi, jumlah molekul gas karbon dioksida sebesar 1,8 × 10²⁴ molekul.
d. Rumus perbandingan jumlah molekul seperti dibawah ini.
Untuk jawaban e sampai g bisa menggunakan rumus perbandingan volume.
e. Rumus perbandingan volume seperti dibawah ini.
Jadi, volume gas oksigen sebesar 21 L.
f. Rumus perbandingan volume seperti dibawah ini.
Jadi, volume gas karbon dioksida sebesar 12 L.
g. Rumus perbandingan volume seperti dibawah ini.
Jadi, volume uap air sebesar 18 L.
Contoh soal No 6 sampai 10 dilanjut disini.
Contoh Soal dan Pembahasan Lengkap Stoikoimetri Kimia (1) - Mungkin sekian dulu ya Contoh Soal dan Pembahasan Stoikoimetri Kimia no 1 sampai 5. Semoga contoh soal dan pembahasan singkat diatas dapat bermanfaat bagi teman setia Sains Seru. Jika ada yang mau ditanyakan bisa tinggalkan di kolom komentar dibawah ya. Kita akan melanjutkan ke Evaluasi Materi BAB jadi ikuti terus ya update artikel disini ya. Terimakasih atas perhatiannya, See You.