Mengenal Senyawa Hidrokarbon di Kimia Kelas 10 SMA - Selamat malam teman Sains Seru, pada kesempatan kali ini kita akan membahas materi baru tentang Senyawa Hidrokarbon. Materi senyawa hidrokarbon ini banyak sekali kaitannya dengan kehidupan sehari-hari, misalnya sebuah intan. Intan merupakan salah satu dari batu mulia, intan juga bisa diolah menjadi perhiasan seperti berlian yang sangat indah. Bukan hanya itu, intan juga bisa di manfaatkan menjadi bor karena memang strukturnya rapat dan keras.
Intan tersusun atas atom-atom karbon yang membentuk struktur geometri tetrahedral. Intan ini adalah salah satu dari contoh senyawa hidrokarbon. Selain intan masih banyak benda yang di dalamnya terdapat atom karbon. Atom karbon juga sering berikatan dengan atom lainnya, tetapi yang paling banyak atom karbon berikatan dengan atom hidrogen membentuk senyawa hidrokarbon seperti senyawa metana (CH₄).
 |
| Google Image - Mengenal Senyawa Hidrokarbon di Kimia Kelas 10 SMA |
Senyawa Hidrokarbon
Hidrokarbon adalah senyawa organik yang hanya mengandung unsur karbon dan hidrogen. Hidrokarbon bukan hanya memiliki dua unsur saja, melainkan memiliki senyawa lain seperti CH₄, C₂H₂, C₂H₄ dan lain-lainnya.
Cara Menguji Unsur C, H, dan O dalam Senyawa
Untuk mengetahui bahwa di dalam suatu senyawa tersebut terdapat unsur C, H, dan O maka dapat menggunakan cara sebagai berikut:
a. Reaksi Pembakaran Senyawa Karbon
Sukrosa atau sering disebut gula pasir merupakan salah satu contoh senyawa karbon, dimana gula pasir memiliki rumus kimia C₁₂H₁₂O₁₁. Jika dibakar, maka gula pasir akan menghasilkan CO₂ dan H₂O dengan persamaan reaksi sebagai berikut.
C₁₂H₁₂O₁₁ + 12 O₂ → 12 CO₂ + 11 H₂O.
b. Cara Menguji Keberadaan Unsur C, H, dan O
Untuk mengetahui dalam suatu senyawa terdapat unsur C, H, dan O bisa menggunakan uji air kapur dan uji kertas kobalt. Uji air kapur disini digunakan untuk mengetahui adanya gas CO₂. Ini menunjukkan bahwa dalam senyawa tersebut terdapat unsur C dan O. Cara menguji dengan air kapur yaitu dengan melewatkan gas CO₂ yang terbentuk ke dalam larutan kapur. Sehingga larutan kapur yang awalnya bening akan berubah menjadi keruh seperti ditunjukkan pada gambar dibawah ini.
Sedangkan uji kertas kobalt digunakan untuk menguji adanya senyawa H₂O. Ini menunjukkan bahwa di dalam senyawa tersebut terdapat unsur H dan O. Cara mengujinya yaitu dengan menyentuhkan kertas kobalt pada uap air hasil pembakaran senyawa karbon. Jika senyawa tersebut terdapat air maka akan berubah warna yang awalnya biru menjadi merah jambu seperti pada gambar dibawah ini.
Penggolongan Berdasarkan Struktur Molekul
Senyawa hidrokarbon dapat di golongkan menjadi 3 berdasarkan struktur molekulnya yaitu:
a. Senyawa Hidrokarbon Alifatik
Senyawa hidrokarbon alifatik adalah senyawa hidrokarbon dengan struktur rantai karbon terbuka. Senyawa yang termasuk ke dalam senyawa hidrokarbon alifatik adalah:
1. Alkana : metana (CH₄), etana (C₂H₆), propana (C₃H₈) dan lain-lain.
2. Alkena : etena (C₂H₄), propena (C₃H₆), butena (C₄H₈) dan lain-lain.
3. Alkuna : etuna (C₂H₂), propuna (C₃H₄), butuna (C₄H₆) dan lain-lain.
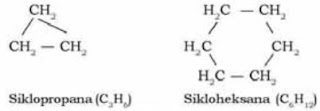
b. Senyawa Hidrokarbon Alisiklik
Senyawa hidrokarbon alisiklik adalah senyawa hidrokarbon yang memiliki struktur rantai karbon tertutup. Contoh dari senyawa hidrokarbon alisiklik adalah:
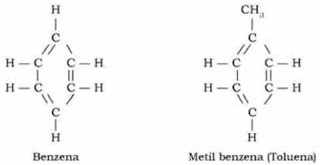
c. Senyawa Hidrokarbon Aromatik
Senyawa hidrokarbon aromatik adalah senyawa hidrokarbon yang memiliki rantai karbon tertutup dan mengandung dua atau lebihikatan rangkap yang letaknya berselang-seling. Contoh dari senyawa hidrokarbon aromatik adalah:
Penggolongan Berdasarkan Kejenuhan Ikatan
Senyawa hidrokarbon dapat di golongkan menjadi 2 berdasarkan kejenuhan ikatan yaitu:
a. Senyawa Hidrokarbon Jenuh
Senyawa hidrokarbon jenuh mempunyai ciri antaratom C berikatan tungga (C ⎯ C). Senyawa yang termasuk kedalam senyawa hidrokarbon jenuh adalah:
1. Golongan Alkana
CH₃ ⎯ CH₃ : Etana (C₂H₆)
CH₃ ⎯ CH₂ ⎯ CH₃ : propana (C₃H₈)
2. Golongan Sikloalkana
b. Senyawa Hidrokarbon tidak Jenuh
Senyawa hidrokarbon tidak jenuh mempunyai ciri antaratom C ada yang berikatan rangkap dua (C = C) dan rangkap tiga (C ≡ C). Senyawa yang termasuk kedalam senyawa hidrokarbon tidak jenuh adalah:
1. Golongan Alkena
CH₂ = CH₂ : Etena (C₂H₄)
CH₂ = CH ⎯ CH₃ : propena (C₃H₆)
2. Golongan Alkuna
CH ≡ CH : Etuna (C₂H₂)
CH ≡ C ⎯ CH₃ : propuna (C₃H₄)
3. Golongan Aromatik
Penggolongan Berdasarkan Tata Nama
Penamaan senyawa hidrokarbon bergantung pada jenis ikatan dan jumlah atom karbonnya. Awalan senyawa hidrokarbon ditentukan dari jumlah atom C-nya. Agar lebih jelasnya kita berikan gambar jumlah atom dan penamaannya sebagai berikut.
Sedangkan untuk penamaan senyawa hidrokarbon dapat diketahui dari jenis ikatannya. Ikatan yang dari senyawa hidrokarbon secara umum dan akhiran nama senyawa hidrokarbon adalah sebagai berikut:
Mengenal Senyawa Hidrokarbon di Kimia Kelas 10 SMA - Demikianlah pembahasan singkat dari materi awal kita tentang Mengenal Senyawa Hidrokarbon di Kimia Kelas 10 SMA. Semoga artikel kali ini bisa bermanfaat ya bagi teman setia Sains Seru. Jika terdapat pertanyaan terkait materi hidrokarbon bisa dituliskan di kolom komentar ya. Untuk artikel depan kita akan membahas Keunikan Atom Karbon dalam Senyawa Hidrokarbon. Jadi ikuti terus ya update artikel disini, terimakasih atas perhatiannya sampai ketemu di artikel selanjutnya ya.